Los argumentos del Invima para autorizar el uso de la vacuna de Pfizer
Para el instituto la coyuntura actual generada a nivel mundial por la pandemia, hacía urgente la aprobación del uso de emergencia de este inmunizante.

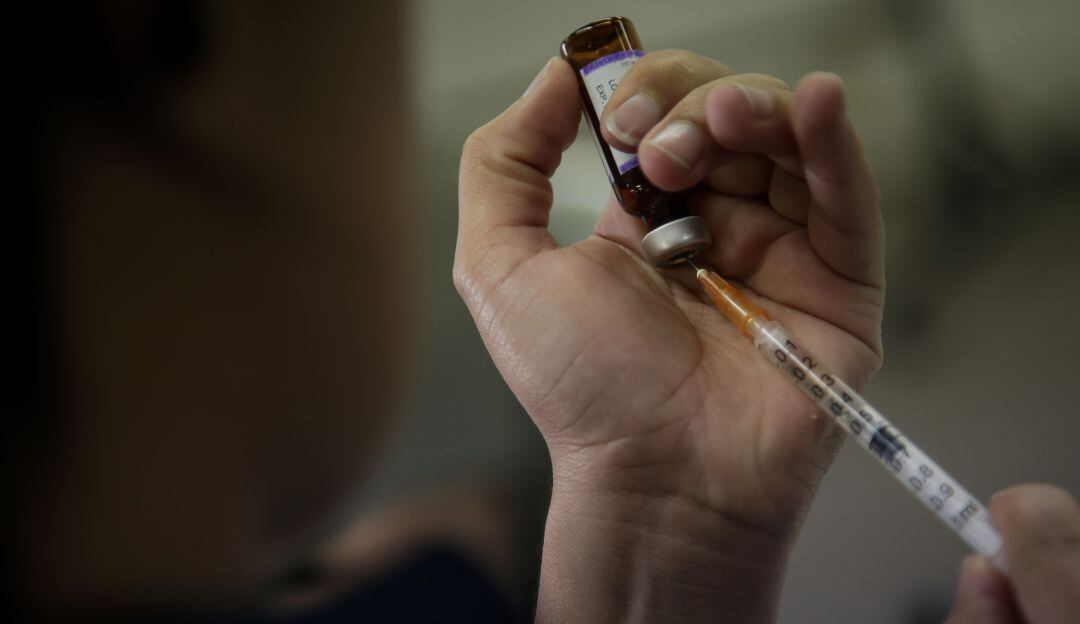
Los argumentos del Invima para autorizar el uso de la vacuna de Pfizer / Mauricio Alvarado (Colprensa)
A través de la resolución 2021000183 del 5 de enero, el Instituto de Nacional de Vigilancia de Medicamentos y Alimentos (INVIMA) otorgó esta primera Autorización Sanitaria de Uso de Emergencia a la vacuna contra el COVID-19 que fue desarrollada por la farmacéutica estadounidense Pfizer.
La sala especializada de medicamentos, que fue la que evaluó los 23 mil folios presentados por Pfizer, consideró que por el momento coyuntural de la pandemia, la morbimortalidad y la afectación del desarrollo social y económico de cada nación, era necesaria esta aprobación "acelerada y condicionada de medicamentos que en fases tempranas de investigación sugieren fuertemente un balance riesgo beneficio favorable".
Le puede interesar:
- Viajeros que ingresen al país podrán no presentar prueba de COVID negativa
- Más de 22 mil trabajadores de la Salud contagiados de COVID-19 en Colombia
La autorización se otorgó por el término de un año, y está condicionada a los nuevos conocimientos que surjan en relación con la seguridad y eficacia del inmunizante, que se obtengan de los estudios clínicos en curso, de los que se van a desarrollar, y de la experiencia clínica que se va acumulando a través de su uso a nivel internacional.
Ahora bien, las condiciones de venta de este medicamento biológico serán de fórmula médica, y se deben garantizar las condiciones de su almacenamiento entre -80 °C y -60 °C por 6 meses, o entre 2 °C y 8 °C por un máximo de 5 días. "Su promoción y publicidad se encuentran prohibidas, al igual que la existencia de muestras médicas o de obsequios del medicamento", añadió y enfatizó el instituto.
Finalmente, precisaron que "la autorización es distinta al registro sanitario, al ser una autorización temporal y condicionada que permite el uso de medicamentos biológicos o de síntesis química que aún no cuentan con toda la información requerida para la obtención de un registro sanitario y que cumplan con los requisitos mínimos de calidad, seguridad y eficacia exigidos".