Invima pidió la suspensión de uso de dos lotes de Propofol inyectable
La alerta se da, según la autoridad sanitaria tras detectarse posibles errores en la producción del medicamento.

Propofol(Getty-images)
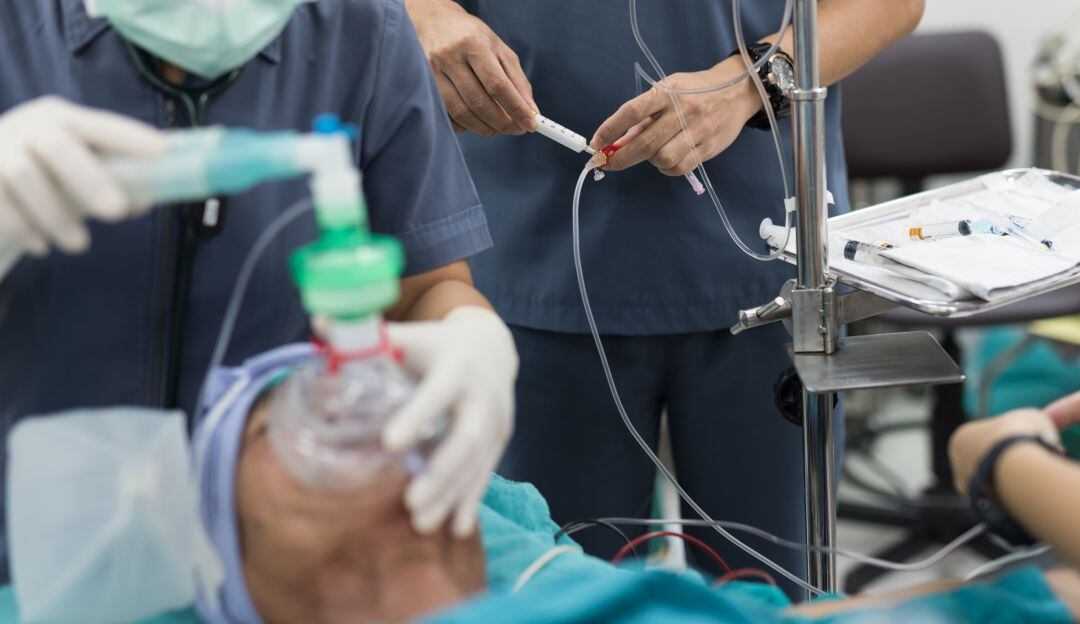
El Invima emitió una alerta sanitaria, exigiendo la suspensión del uso y comercialización del Propofol en presentación inyectable de 10 miligramos y 10 mililitros, el que viene en cajas de un vial o un frasco, del fabricante Biozenta Life Science de la India, el cual a propósito ingresó al país, bajo la figura de vital no disponible debido a la escasez que se presenta de anestésicos y sedantes indispensables para el tratamiento de pacientes en Unidades de Cuidado Intensivo.
En detalle, este medicamento, habitualmente se usa para la sedación de pacientes adultos sometidos a ventilación mecánica o para procedimientos invasivos cortos.
La orden de retiro recae sobre los lotes GI21002-GI21001, luego de que así lo solicitara el mismo titular autorizado para importarlo, tras detectar posibles errores en el proceso de producción de algunas muestras del medicamento.

Yorely Ibarguen
Editora y periodista de la información de Salud, Educación y Medio Ambiente desde 2019. Ha estado al...