Pfizer pidió autorización al Invima para el uso de su vacuna en el país
Tras la solicitud de emergencia enviada por la farmacéutica, el Invima cuenta ahora con diez días hábiles para pronunciarse sobre esta autorización.

Pfizer podría convertirse en la primera vacuna avalada para el Gobierno nacional. / Getty Images
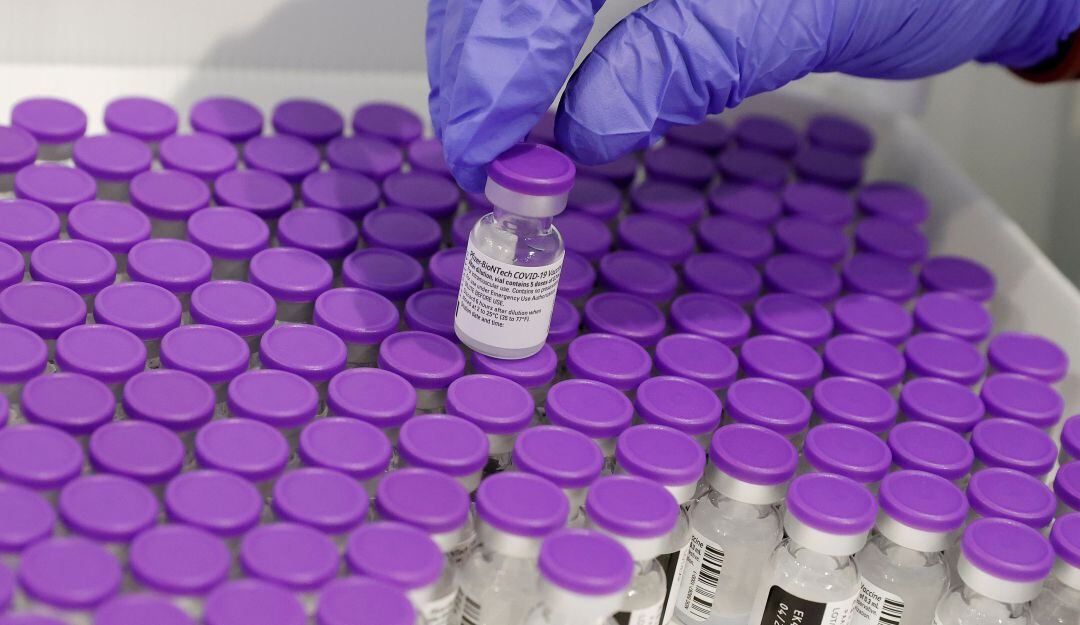
La farmacéutica estadounidense Pfizer ya le solicitó al Invima, Instituto Nacional de Vigilancia de Medicamentos y Alimentos, la autorización sanitaria para el uso de emergencia de la vacuna contra el COVID-19 producida por esta firma con la con la empresa de biotecnología alemana BioNTech.
Ester 31 de diciembre fueron radicados los documentos ante la autoridad sanitaria que ahora tendrá 10 días hábiles para que su sala especializada de medicamentos evalúe la información y pueda emitir un pronunciamiento de fondo acerca de la petición de emergencia.
De ser aprobada en este plazo, máximo hasta el 18 de enero, el antídoto de Pfizer se convertirá en la primera vacuna en todo el país en lograr este aval, siendo evidentemente el primer paso para dar inicio al Plan Nacional de Vacunación anunciado por el Ministerio de Salud.
Este antídoto, que ya ha sido arobado y utilizado en más de 50 países, ha demostrado también una eficacia del 95%, se aplican dos dosis por persona, y ha sido destacado por expertos por la alta seguridad en su uso. El Gobierno colombiano tiene negociadas actualmente 10 mil dosis con esta farmacéutica, que servirán entonces para inmunizar a cinco millones de colombianos, una vez se apruebe.