Los procesos de autorización de vacunas bivalentes COVID-19 están estancados en el Invima
Caracol Radio conoció que dos farmacéuticas han presentado solicitud para uso de emergencia de estos biológicos.
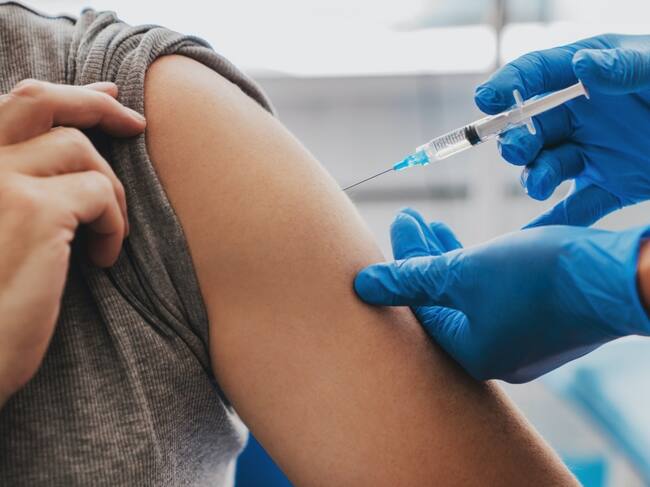
Imagen de archivo - Gobernación de Risaralda.
Desde finales del año pasado, la farmacéutica Moderna presentó ante el Invima una solicitud de Autorización de Uso de Emergencia (ASUE) de su vacuna Spikevax Bivalent. Según le confirmó el Instituto Nacional de Vigilancia de Medicamentos (Invima) a Caracol Radio, todavía no se ha otorgado la autorización para aplicarse en el país. De acuerdo a las bases de datos del Invima, esta vacuna se encuentra “agendada para estudio de la Comisión Revisora de Seguridad y Eficacia”.
Además, Caracol Radio pudo establecer que, el laboratorio Pfizer también realizó una solicitud de uso de emergencia para su vacuna bivalente ante el Invima. Este biológico se denomina Comirnaty y se encuentra estancado en el mismo punto del proceso de autorización. Agendado para revisión.
Sin embargo, no se específica cuando podría darse esta verificación de parte del área responsable de la revisión. Se debe recordar que, estas vacunas son las de última tecnología y las más eficaces contra las variantes de Ómicron del Coronavirus.
Finalmente, conocimos que 6 de las 7 vacunas contra el Covid-19 en el país tienen su autorización de uso de emergencia vigente, por ahora AstraZeneca está pendiente de renovar este aval en el país y ya empezó el trámite. .