Pfizer solicitó el registro definitivo de su vacuna en Brasil
Esto con el objetivo de comercializarla y utilizarla de forma generalizada, informó el regulador sanitario del país sudamericano

. (Getty Images)
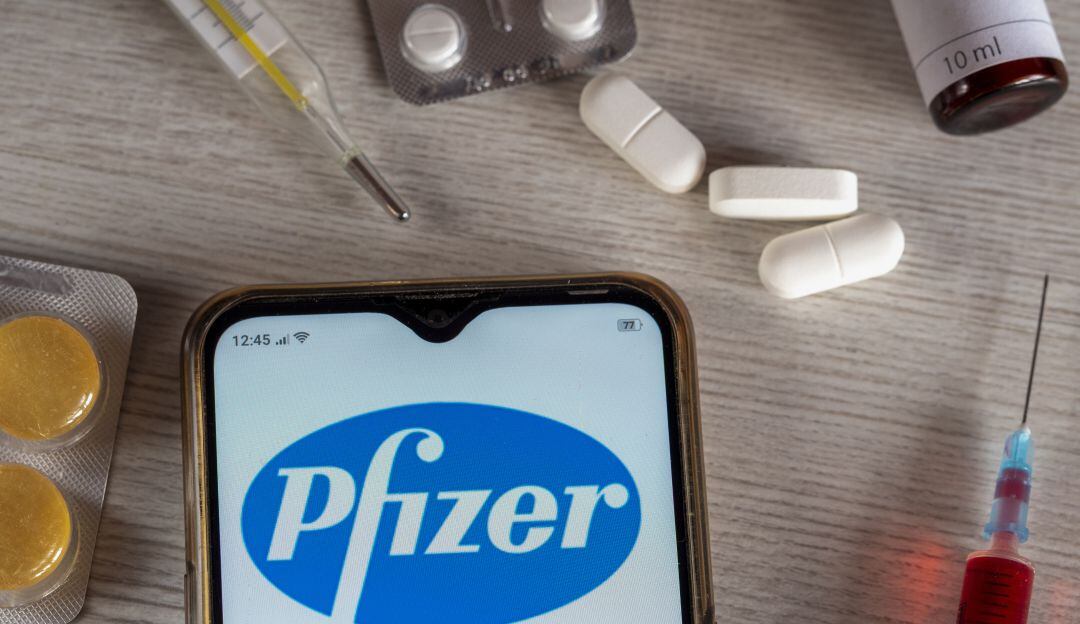
El laboratorio estadounidense Pfizer pidió este sábado en Brasil el registro definitivo de su vacuna contra el coronavirus para poder comercializarla y utilizarla de forma generalizada, informó el regulador sanitario del país sudamericano.
La Agencia Nacional de Vigilancia Sanitaria de Brasil (Anvisa) precisó que cuando apruebe la solicitud, Cominarty, como se llama la vacuna de Pfizer, podrá ser "comercializada, distribuida y utilizada por la población en los términos establecidos en el prospecto".
Este es el segundo pedido para uso definitivo formalizado ante Anvisa en Brasil. El primero fue presentado por el británico AstraZeneca/Oxford y el brasileño Instituto Fiocruz en enero.
Leer más: Inicia la capacitación para vacunación contra COVID-19 en Cundinamarca
Leer más: El pasaporte verde en Israel que diferencia a personas vacunadas
La nueva solicitud se produjo en momentos en que el país de 212 millones de habitantes vive un recrudecimiento de la pandemia.
Con más de 1.200 muertes registradas en las últimas 24 horas, Brasil totaliza más de 230.000 óbitos y 9,4 millones de contagios de COVID-19. La situación se agudiza en varios estados del norte del país, como Amazonas, donde el sistema de salud se encuentra colapsado.
Hasta ahora, Anvisa solo aprobó el uso de emergencia de 2 millones de dosis importadas de la vacuna AstraZeneca/Oxford (producida junto a Fiocruz) y de unos 10 millones de la CoronaVac, desarrollada por la biotecnológica china Sinovac en asociación con el Instituto Butantan de Sao Paulo. Ambas requieren dos dosis por persona.
En su comunicado, Anvisa no establece un plazo para responder la solicitud, sin embargo anteriormente ha fijado un lapso de 60 días para analizar los documentos.
"Anvisa viene evaluando de forma de emergencia y con total prioridad las vacunas contra covid-19", agrega en la nota divulgada este sábado.Brasil inició hace tres semanas su campaña de inmunización que avanza de forma gradual, centrada primero en el personal de la salud, los ancianos y la población indígena.
Más de 3 millones de personas han sido vacunados en Brasil hasta ahora.